美国食品药品管理局 (FDA) 已批准 Magstim 的 Horizon ® 3.0 Inspire 用于治疗之前使用抗抑郁药物后症状没有得到满意改善的成人重度抑郁症 (MDD)。该疗法还可作为成人强迫症 (OCD) 的辅助治疗。
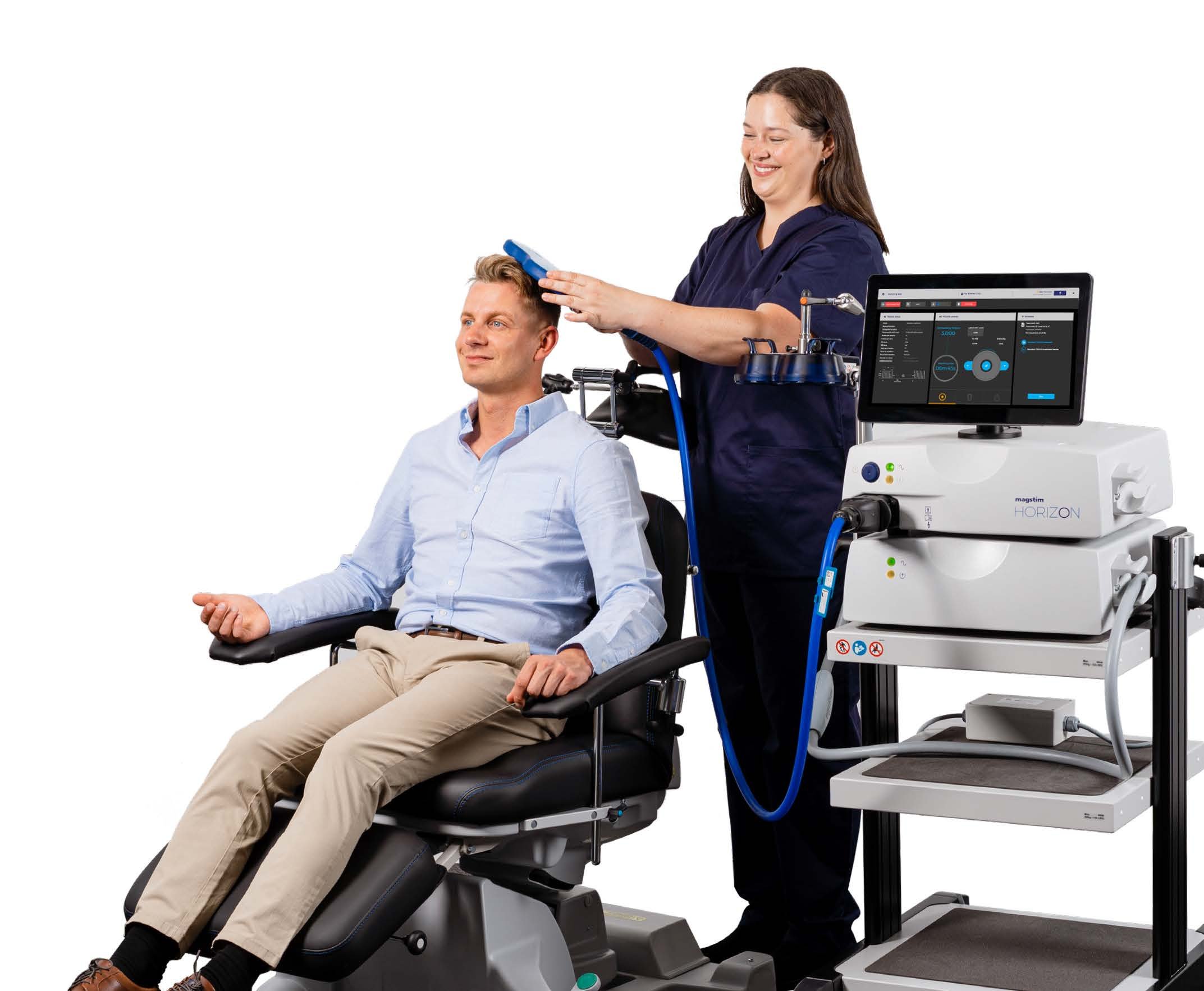
Horizon 3.0 经颅磁刺激 (TMS) 治疗系统是一种计算机化的非侵入式医疗设备,可将电流引导至大脑皮层的不同区域。该系统由一个装置和电源、用户界面、用于运动阈值的施加线圈、用于治疗的施加线圈以及系统和施加线圈推车和支撑臂组成。该设备只能在住院和门诊环境中在医生的监督下凭处方使用。
Horizon 3.0 TMS 治疗系统有 3 种不同的配置,包括之前已获批准的 Horizon 3.0 和带 StimGuide Pro 的 Horizon 3.0,以及现已获批准的 Horizon 3.0 Inspire。所有系统都具有相同的使用指征、主要组件、操作原理和技术特点。
据该公司称,此次批准是基于非临床测试的结果,该测试证明其安全性和有效性与主要预测设备 Horizon 3.0 和 Horizon 3.0 with StimGuide Pro 相当。非临床测试包括电磁兼容性、电气、机械和热安全性、软件验证和确认、可用性、磁脉冲输出和磁场和电场测试、安全特性测试和声学测试。
Horizon 3.0 Inspire 升级了空气冷却线圈技术,可实现连续治疗,并通过预设的临床工作流程优化治疗过程。此外,该设备设计紧凑,便于携带。
Magstim 首席执行官 Ronnie Stolec-Campo 表示:“医生、执业护士和心理健康护理专家告诉我们,患者正在寻找药物治疗的替代品。FDA 批准的经颅磁刺激是一种经过验证的有效治疗方法,副作用极小。我们设计 Inspire 是为了既能为经验丰富的 TMS 提供者服务,也能为 TMS 新手服务。”
参考来源:‘FDA clears Magstim Horizon Inspire transcranial magnetic stimulation system to treat depression, OCD, anxious depression. News release. Magstim Company Ltd. November 12, 2024.’
注:本文旨在介绍医药健康研究,不作任何用药依据,具体用药指引,请咨询主治医师。
(责任编辑:登越药房)




