Asciminib的商品名为Scemblix,是一种用于治疗费城染色体阳性慢性粒细胞白血病(Ph+ CML) 的药物。 Asciminib 是一种蛋白激酶抑制剂。
Asciminib 于 2021 年 10 月在美国获准用于医疗用途,并于 2022 年 8 月在欧盟获准用于医疗用途。
【适用病症】
白血病
【生产厂家】
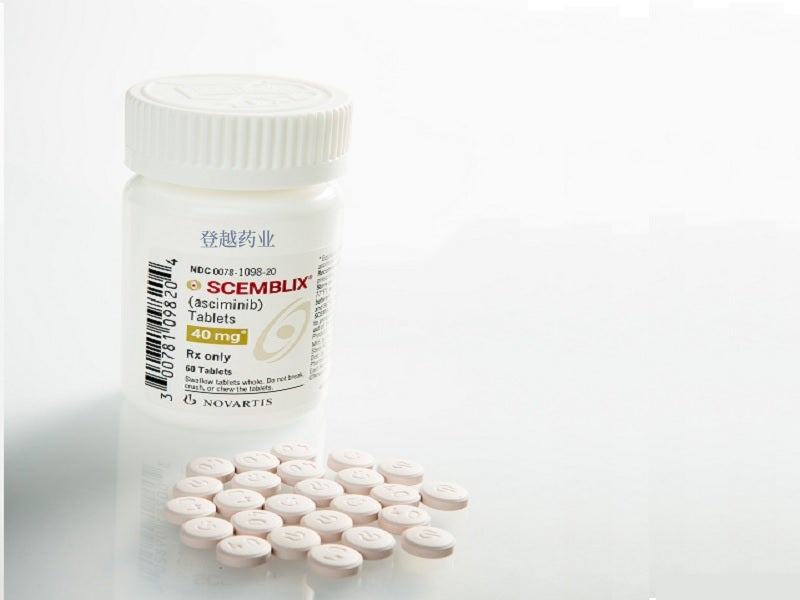
瑞士诺华制药
【药品规格】
40mg*60片 20mg*60片
【商品名称】
Scemblix
【英文名称】
sciminib
【中文名称】
阿西米尼
【全部名称】
Scemblix、asciminib、阿西米尼
【适应症】
SCEMBLIX适用于治疗患有以下疾病的成人患者:
1、费城染色体阳性慢性髓性白血病(Ph+ CML),慢性期(CP),既往接受过两种或两种以上酪氨酸激酶抑制剂(tki)治疗。
2、出现T315I突变的CP中Ph+ CML。
【用法用量】
1、先前接受过两次或多次tki治疗的Ph+ CML-CP患者的推荐剂量
Scemblix(asciminib)的推荐剂量为80 mg口服,每日一次,每天服药时间大致相同,或40 mg口服,每日两次,间隔约12小时。推荐剂量的SCEMBLIX可在不进食的情况下口服。至少在服用SCEMBLIX前2小时和服用SCEMBLIX后1小时内避免进食。
只要观察到临床获益或直到出现不可接受的毒性,就继续使用SCEMBLIX治疗。
2、2T315I突变的Ph+ CML-CP患者的推荐剂量
Scemblix(asciminib)的推荐剂量为200 mg,口服,每日两次,间隔约12小时。推荐剂量的Scemblix(asciminib)可在不进食的情况下口服。至少在服用SCEMBLIX前2小时和服用Scemblix(asciminib)后1小时内避免进食。
3、漏服剂量
每日一次给药方案:如果错过Scemblix(asciminib)剂量超过约12小时,则跳过该剂量,并按计划服用下一剂量。
每日两次给药方案:如果错过Scemblix(asciminib)剂量超过约6小时,则跳过该剂量并按计划服用下一剂量。
【副作用】
最常见的不良反应 (≥ 20%) 是上呼吸道感染、肌肉骨骼疼痛、疲劳、恶心、皮疹和腹泻。
【作用机制】
阿西米尼布属于一类叫做激酶抑制剂的药物,它通过阻断信号癌细胞繁殖的异常蛋白质的作用而起作用,这有助于阻止癌细胞的扩散。
【注意事项】
1、骨髓抑制
接受Scemblix(asciminib)治疗的患者出现血小板减少、中性粒细胞减少和贫血。在356名接受Scemblix(asciminib)治疗的患者中,有98名(28%)出现血小板减少症,分别有24名(7%)和42名(12%)患者报告有3级或4级血小板减少症。在3级或4级血小板减少症患者中,事件首次发生的中位时间为6周(范围:0.1至64周)。在98例血小板减少症患者中,7例(2%)患者永久停用sceblux,45例(13%)患者因不良反应暂时停用Scemblix(asciminib)。
接受Scemblix(asciminib)治疗的69例(19%)患者出现中性粒细胞减少,分别有26例(7%)和30例(8%)患者报告3级和4级中性粒细胞减少。在3级或4级中性粒细胞减少症患者中,事件首次发生的中位时间为6周(范围:0.1至180周)。在69例中性粒细胞减少症患者中,4例(1.1%)患者永久停用Scemblix(asciminib),34例(10%)患者因不良反应暂时停用sceblux。
接受Scemblix(asciminib)治疗的46名(13%)患者发生贫血,其中19名(5%)患者发生3级贫血。在3级或4级贫血患者中,事件首次发生的中位时间为30周(范围:0.4至207周)。在46例贫血患者中,有2例(0.6%)患者因不良反应而暂时停用Scemblix(asciminib)[参见“不良反应”]。
在前3个月的治疗中,每两周进行一次全血细胞计数,之后每月或根据临床指示进行一次。监测患者骨髓抑制的体征和症状。
根据血小板减少症和/或中性粒细胞减少症的严重程度,减少剂量、暂时停用或永久停用sceblux[参见“剂量和用法”]。
2、胰腺毒性
在接受Scemblix(asciminib)治疗的356例患者中,有9例(2.5%)发生胰腺炎,其中4例(1.1%)发生3级胰腺炎。所有胰腺炎病例均发生在I期研究(X2101)中。在9例胰腺炎患者中,2例(0.6%)患者永久停用sceblux,4例(1.1%)患者因不良反应暂时停用Scemblix(asciminib)。在接受Scemblix(asciminib)治疗的356例患者中,76例(21%)出现无症状的血清脂肪酶和淀粉酶升高,其中36例(10%)和8例(2.2%)患者分别出现3级和4级胰酶升高。在76例胰酶升高的患者中,有8例(2.2%)患者因不良反应而永久停用Scemblix(asciminib)[参见“不良反应”]。
在Scemblix(asciminib)治疗期间或按照临床指示每月评估血清脂肪酶和淀粉酶水平。监测患者胰腺毒性的体征和症状。对有胰腺炎病史的患者进行更频繁的监测。如果脂肪酶和淀粉酶升高伴有腹部症状,则暂时停用Scemblix(asciminib),并考虑进行适当的诊断试验以排除胰腺炎[参见“剂量和用法”]。
根据脂肪酶和淀粉酶升高的严重程度,减少剂量、暂时停用或永久停用sceblux[参见“剂量和用法”]。
3、高血压
在接受Scemblix(asciminib)治疗的356名患者中,有68名(19%)发生高血压,分别有32名(9%)和1名(0.3%)患者报告有3级或4级高血压。3级或4级高血压患者首次发病的中位时间为14周(范围:0.1至156周)。在68例高血压患者中,有3例(0.8%)患者由于不良反应而暂时停用Scemblix(asciminib)[参见“不良反应”]。
在Scemblix(asciminib)治疗期间,根据临床指示,使用标准抗高血压治疗监测和管理高血压;对于3级或更高的高血压,根据高血压的持续情况,暂时停用、减少剂量或永久停用SCEMBLIX[参见“剂量与用法”]。
4、超敏反应
在接受Scemblix(asciminib)治疗的356名患者中,有115名(32%)发生超敏反应,6名(1.7%)患者报告有3级或4级超敏反应[参见“不良反应”(6.1)]。反应包括皮疹、水肿和支气管痉挛。监测患者的超敏反应体征和症状,并根据临床指示开始适当治疗;对于3级或更高的超敏反应,根据超敏反应的持续情况,暂时停止、减少剂量或永久停用Scemblix(asciminib)[参见“剂量与给药”]。
5、心血管毒性
在接受SCEMBLIX治疗的356名患者中,分别有46名(13%)和9名(2.5%)出现心血管毒性(包括缺血性心脏和CNS疾病、动脉血栓形成和栓塞疾病)和心力衰竭[参见“不良反应”(6.1)]。12例(3.4%)患者报告了3级心血管毒性,5例(1.4%)患者报告了3级心力衰竭。2例(0.6%)患者发生4级心血管毒性,3例(0.8%)患者发生死亡。3例(0.8%)患者因心血管毒性永久停用Scemblix(asciminib),1例(0.3%)患者因心力衰竭永久停用SCE mblix。心血管毒性发生于已有心血管疾病或风险因素和/或之前接触过多种tki的患者。
在356名接受Scemblix(asciminib)治疗的患者中,有24名发生心律失常(包括QTc延长),其中8名(2%)患者报告有3级心律失常。在接受Scemblix(asciminib)治疗的356名患者中,有3名(0.8%)出现QTc延长,1名(0.3%)患者报告出现3级QTc延长[参见“不良反应”]。
监测有心血管危险因素史的患者的心血管体征和症状。根据临床指示开始适当治疗;对于3级或更高心血管毒性,根据心血管毒性的持续性,暂时停止、减少剂量或永久停用Scemblix(asciminib)[参见“剂量与给药”]。
6、胚胎-胎仔毒性
根据动物研究的结果及其作用机制,Scemblix(asciminib)在对孕妇给药时会对胎儿造成伤害。在动物生殖研究中,在器官发生期间对妊娠大鼠和兔给予阿西米尼会导致不良发育结局,包括母体暴露量(AUC)等于或小于推荐剂量时患者的胚胎-胎仔死亡率和畸形。如果在妊娠期间使用sceblux或如果患者在服用Scemblix(asciminib)期间怀孕,则告知具有生殖潜力的孕妇和雌性对胎儿的潜在风险。在开始Scemblix(asciminib)治疗前,验证具有生殖潜力的雌性的妊娠状态。有生殖潜力的雌性应在Scemblix(asciminib)治疗期间和最后一次给药后1周内使用有效避孕方法[参见“特定人群中的使用”]。
【特殊人群用药】
1、怀孕
根据动物研究的结果和作用机制,对孕妇给药时,Scemblix(asciminib)可造成胚胎-胎仔伤害。没有关于孕妇使用Scemblix(asciminib)评估药物相关风险的可用数据。
在妊娠大鼠和兔中进行的动物生殖研究表明,在器官发生过程中口服阿西米尼会诱发结构异常、胚胎-胎仔死亡率和生长变化。
告知孕妇和有生殖潜力的女性对胎儿的潜在风险。
2、哺乳期
目前还没有关于Scemblix(asciminib)或其代谢产物在人乳中的存在、对母乳喂养儿童的影响或产奶量的数据。
由于母乳喂养的婴儿可能出现严重的不良反应,建议妇女在服用Scemblix(asciminib)治疗期间和末次给药后1周内不要进行母乳喂养。
3、具有生殖潜力的男性和女性
根据动物研究的结果,当对孕妇给药时,Scemblix(asciminib)可导致胚胎-胎仔伤害[参见“在特定人群中的使用”]。
在开始Scemblix(asciminib)治疗前,验证具有生殖潜力的雌性的妊娠状态。
在Scemblix(asciminib)治疗期间和末次给药后1周内,有生殖潜力的女性应使用有效避孕方法。
根据动物研究结果,Scemblix(asciminib)可能会损害具有生殖潜力的女性的生育能力。这种效应对生育力的可逆性尚不清楚。
4、儿童用药
尚未确定Scemblix(asciminib)在儿科患者中的安全性和疗效。
5、老年用药
总体而言,与年轻患者相比,未观察到65岁及以上患者服用Scemblix(asciminib)的安全性或疗效存在差异。75岁及以上的患者人数不足以评估安全性或疗效是否存在差异。
6、肾功能损害
对于轻度至重度肾功能损害(肾小球滤过率估计值[eGFR] 15至89 mL/min/1.73 m2)且无需接受SCEMBLIX透析的患者,无需调整剂量。
7、肝功能损害
对于接受Scemblix(asciminib)治疗的轻度[总胆红素≤正常上限(ULN)和天冬氨酸转氨酶(AST) > ULN或总胆红素> 1至1.5倍ULN和任何AST]至重度肝功能损害(总胆红素> 3倍ULN和任何AST)的患者,无需调整剂量。
【禁忌症】
无
【药物相互作用】
某些CYP3A4底物
阿西米尼是一种CYP3A4抑制剂。同时使用Scemblix(asciminib)会增加CYP3A4底物的Cmax和AUC,这可能会增加这些底物的不良反应风险。
密切监测接受80 mg每日总剂量Scemblix(asciminib)联合使用某些CYP3A4底物治疗的患者的不良反应,其中最小的浓度变化可能导致严重的不良反应。避免每日两次将200mg SCE mblix与某些CYP3A4底物联合给药,在这种情况下,最小的浓度变化可能会导致严重的不良反应。
CYP2C9底物
阿西米尼是一种CYP2C9抑制剂。同时使用Scemblix(asciminib)会增加CYP2C9底物的Cmax和AUC,这可能会增加这些底物的不良反应风险。
避免每日总剂量为80 mg的Scemblix(asciminib)与某些CYP2C9底物联合给药,在这种情况下,最小的浓度变化可能会导致严重的不良反应。如果联合用药不可避免,请按照其处方信息中的建议减少CYP2C9底物剂量。
避免每日两次200mg Scemblix(asciminib)与敏感CYP2C9底物和某些CYP2C9底物联合给药,在这些情况下,最小的浓度变化可能导致严重的不良反应。如果联合用药不可避免,则考虑使用非CYP2C9底物的替代疗法。
某些P-gp底物
阿西米尼是一种P-gp抑制剂。同时使用Scemblix(asciminib)会增加P-gp底物的血浆浓度,这可能会增加这些底物的不良反应风险。
密切监测所有推荐剂量的Scemblix(asciminib)联合P-gp底物治疗患者的不良反应,其中最小的浓度变化可能导致严重的毒性。
【成分】
本品主要成分为阿西米尼。
【性状】
红色片剂
【贮存方法】
储存温度:20°C至25°C(68°F至77°F);允许在15°C和30°C(59°F和86°F)之间波动[参见USP控制的室温]。
分装并储存在原容器中,以防受潮。
温馨提示:以上资讯由登越药业整理编辑(如有错漏,请帮忙指正),只为提供全球最新上市药品的资讯,帮助中国患者了解国际新药动态,仅供医护人员内部讨论,不作任何用药依据,具体用药指引,请咨询主治医师。
(责任编辑:登越药房)




