英国药监机构(MHRA)已批准糖尿病和体重管理药物Mounjaro(tirzepatide)的四剂版本(涵盖一个月的治疗)——Mounjaro KwikPen,预计将在数周内上市。
英国药监机构(MHRA)已批准糖尿病和体重管理药物Mounjaro(tirzepatide)的四剂版本(涵盖一个月的治疗)——Mounjaro KwikPen,预计将在数周内上市。
英国将成为第一个以多针笔式注射器形式供应该药物的主要市场。在欧盟,KwikPen版本还在监管审查中。
与去年MHRA批准的早期单剂量版本一样,Mounjaro KwikPen被批准用于治疗成人2型糖尿病,和BMI为30kg/m²或以上(肥胖)、以及BMI为27-30kg/m²(超重)且患有与体重相关的健康问题(如糖尿病前期、高血压、高胆固醇或心脏问题)的成人患者的体重管理。
该药物应与减少热量饮食和增加体力活动结合使用。
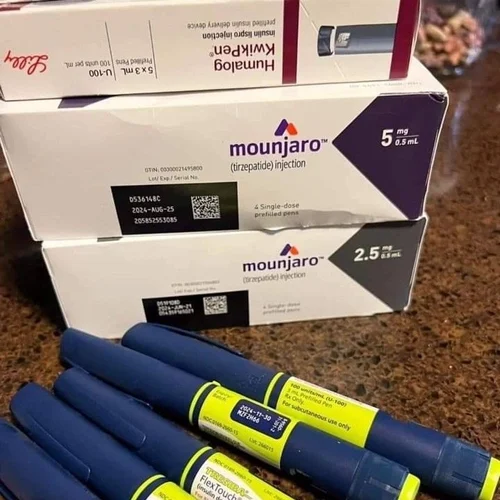
Mounjaro KwikPen是一种四剂量预充式注射笔,每剂量含有2.5毫克、5毫克、7.5毫克、10毫克、12.5毫克和15毫克tirzepatide,在患者胃部、大腿或上臂部位皮下注射。
起始剂量为每周一次2.5毫克,持续四个星期,然后增加至每周一次5毫克。如果患者医生建议,则可以至少每隔4周增加一次剂量,直至每周一次的最大剂量15毫克。
MHRA医疗质量和可及性临时执行董事Julian Beach表示:“这一批准使获得批准的Mounjaro笔能够以更方便的方式提供一个月的治疗,每周一剂。”

Mounjaro是如何工作的
这种疗法中的活性成分tirzepatide只有在血糖水平较高时才有助于降低二型糖尿病患者的血糖水平。它还能调节患者的食欲,让患者感到饱腹、减少饥饿感,以减少对食物的欲望。
证据基础
Mounjaro KwikPen的批准基于桥接研究的结果,该研究提供的证据表明,多剂量Mounjaro KwikPen的功效和安全性预计与基于七项全球临床试验批准的单剂量Mounjaro笔的功效和安全性相同。
其中5项试验(SURPASS1-5)总共涉及6,263名受试者,研究了活性成分tirzepatide对2型糖尿病受试者的安全性和有效性。在所有研究中,与安慰剂或活性对照(司美格鲁肽、德谷胰岛素和甘精胰岛素)相比,接受tirzepatide治疗的受试者的空腹血糖水平显著降低,持续时间长达一年。在一项研究中,这些影响可持续长达两年。体重也显著下降。
其中两项试验(SURMOUNT1-2)总共涉及3,477名受试者,研究了tirzepatide用于患有或不患有糖尿病的超重和肥胖成人进行体重管理(减少和维持)时的安全性和有效性。在这两项研究中,无论年龄、性别、种族、民族、基线体重指数和血糖(状态)如何,与安慰剂相比,接受tirzepatide治疗的超重或肥胖成年人的体重显著降低。
副作用
该药最常见的副作用是恶心、腹泻、呕吐(通常会随着时间的推移而消失)和便秘。低血糖在糖尿病患者中也很常见。症状包括头痛、嗜睡、虚弱、头晕、饥饿感、意识混乱、烦躁、心跳加快和出汗。
使用口服避孕药的肥胖或超重女性患者还应考虑使用屏障避孕方法(如避孕套)或在开始使用Mounjaro后的4周内以及每次增加剂量后的4周内改用非口服避孕方法,因为Mounjaro可能会影响避孕药在这些患者中的效果。
参考来源:‘Four-dose Mounjaro “KwikPen” approved by MHRA for diabetes and weight management’,新闻稿。Medicines and Healthcare products Regulatory Agency
温馨提示:以上资讯由登越药业整理编辑(如有错漏,请帮忙指正),只为提供全球最新上市药品的资讯,帮助中国患者了解国际新药动态,仅供医护人员内部讨论,不作任何用药依据,具体用药指引,请咨询主治医师。
(责任编辑:登越药房)




