2024年5月22日讯/香港登越药业Dengyue/--美国食品药品管理局 (FDA) 已批准 Benlysta (belimumab) 使用自动注射器进行皮下 (SC) 给药,用于接受标准疗法的 5 岁及以上患有活动性系统性红斑狼疮
2024年5月22日讯/香港登越药业Dengyue/--美国食品药品管理局 (FDA) 已批准Benlysta (belimumab) 使用自动注射器进行皮下 (SC) 给药,用于接受标准疗法的 5 岁及以上患有活动性系统性红斑狼疮 (SLE) 的患者。此前,儿童 SLE 患者仅获准接受静脉 (IV) 给药。此选项为儿科患者提供了在家接受治疗的可能性。


此前,五岁及以上儿童只能 通过静脉注射 (IV) 制剂接受贝利尤单抗,由医疗保健专业人员在医院或诊所通过一小时输注,按体重 10 毫克/公斤的剂量向患者给药每四个星期一次(在第 0、14 和 28 天进行初始加载阶段之后)。现在,儿童的医疗保健提供者将确定在家给药是否合适。如果是这样,医疗保健提供者将进行治疗,或者医疗保健提供者将向患者的护理人员提供说明,允许他们在家中通过自动注射器对体重 40 公斤或以上的儿童进行给药,每周一次,或每两周一次体重 15 公斤至 <40 公斤的儿童需几周。
关于狼疮
系统性红斑狼疮 (SLE) 是最常见的狼疮形式,是一种慢性、无法治愈的自身免疫性疾病,伴有一系列随时间波动的症状,包括关节疼痛或肿胀、极度疲劳、不明原因发烧、皮疹和器官损伤。
葛兰素史克公司高级副总裁兼美国专科负责人 Court Horncastle 在新闻稿中表示:“患者是我们的首要任务,我们一直在努力创新解决方案,以改善生活并满足未满足的需求。”“这项针对儿童狼疮的家庭治疗获批是首个也是唯一一个此类治疗,证明了我们对狼疮社区的持续承诺。”
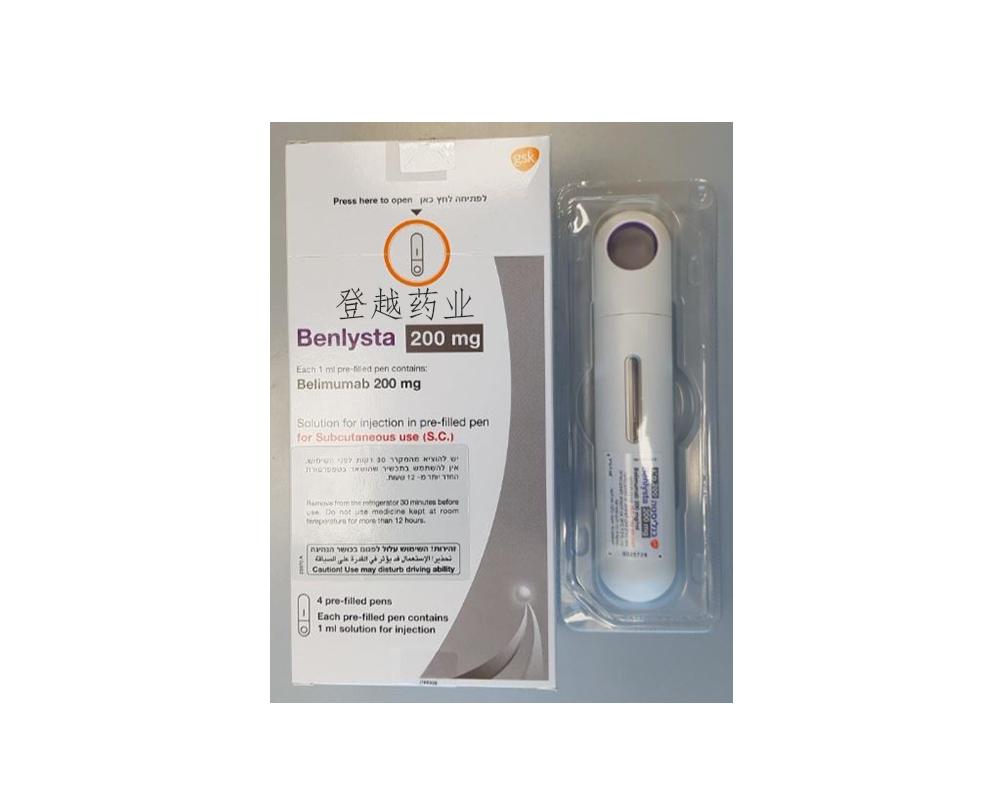
200mg 单剂量预装自动注射器允许儿科患者通过 SC 给药在家接受 SLE 治疗。对于 10 岁以下的患者,自动注射器必须由医疗保健专业人员或经过培训的护理人员进行管理。

该批准得到了一项开放标签药代动力学试验(ClinicalTrials.gov 标识符:NCT04179032)的数据支持,该试验评估了体重至少 15 公斤的 5 至 18 岁儿童 SLE 患者皮下注射 Benlysta 的情况。结果显示,儿科患者皮下注射给药后(200毫克,每周[体重≥40公斤的患者]或每两周[体重15至<40公斤的患者]),稳态平均贝利尤单抗浓度估计与皮下注射后成人的稳态平均浓度相似每周 200mg,与儿科患者静脉注射 Benlysta 10mg/kg 后的情况相似,前 3 剂每 2 周一次,此后每 4 周一次。
与 Benlysta 相关的最常见不良反应包括恶心、腹泻、发热、鼻咽炎、支气管炎、失眠、四肢疼痛、抑郁、偏头痛和咽炎以及注射部位反应(SC 给药)。
Benlysta 是一种 B 淋巴细胞刺激剂 (BLyS) 特异性抑制剂,以单剂量预装自动注射器或预装注射器形式提供,含有 200mg/mL 贝利尤单抗,供皮下注射使用。尚未对 18 岁以下儿童进行预充式注射器的研究。该产品还有 120mg 和 400mg 贝利尤单抗,分别装在 5mL 和 20mL 单剂量小瓶中,供静脉注射使用。
参考来源:FDA approves Benlysta (belimumab) Autoinjector for children with systemic lupus erythematosus. News release. GSK plc. May 20, 2024.
温馨提示:以上资讯来源于网络,由登越药业整理编辑(如有错漏,请帮忙指正),只为提供全球最新上市药品的资讯,帮助中国患者了解国际新药动态,仅供医护人员内部讨论,不作任何用药依据,具体用药指引,请咨询主治医师。
(责任编辑:登越药房)




