2024年5月21日讯/香港登越药业Dengyue/--FDA 批准了 aflibercept-jbvf(Yesafili;Biocon Biologics)和 aflibercept-yszy(Opuviz;Biogen),这是第一个与 aflibercept(Eylea;Regeneron)可互换的生物仿制药。阿柏
2024年5月21日讯/香港登越药业Dengyue/--FDA 批准了 aflibercept-jbvf(Yesafili;Biocon Biologics)和 aflibercept-yszy(Opuviz;Biogen),这是第一个与 aflibercept(Eylea;Regeneron)可互换的生物仿制药。阿柏西普抑制血管内皮生长因子,防止眼内血管异常生长,从而减缓或减少对视网膜的损伤,有助于保护视力。
Yesafili 和 Opuviz 可治疗新生血管性年龄相关性肌肉变性、视网膜静脉阻塞后黄斑水肿、糖尿病黄斑水肿和糖尿病视网膜病变。这两种药物均以 2 mg 注射液形式供患者玻璃体内给药。
阿柏西普产品通过抑制血管内皮生长因子(VEGF)来防止眼睛内的血管异常生长。通过阻断VEGF,阿柏西普产品可以减缓或减少对视网膜的损害,并有助于保护视力。
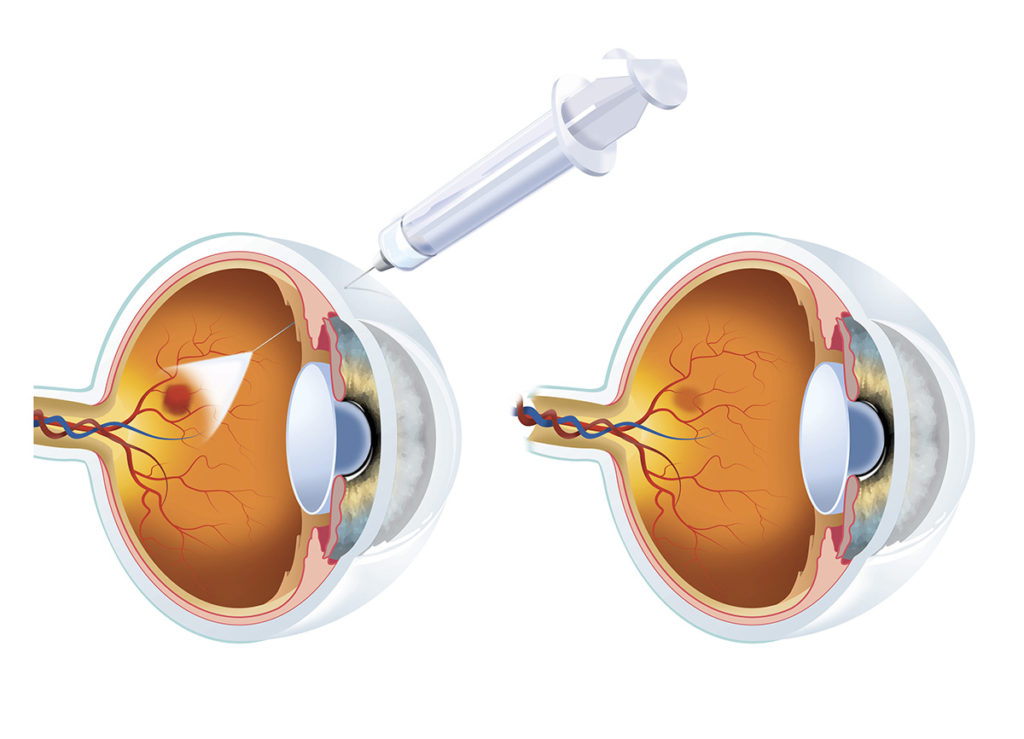
阿柏西普产品通过抑制血管内皮生长因子(VEGF)发挥作用,从而防止眼内血管异常生长。通过阻断 VEGF,阿柏西普产品可以减缓或减少对视网膜的损伤,并有助于保护视力。
Yesafili 和Opuviz均 用于治疗:
l.新生血管性(湿性)年龄相关性黄斑变性
2.视网膜静脉阻塞后黄斑水肿
3.糖尿病黄斑水肿
4.糖尿病性视网膜病变
Yesafili 和 Opuviz 均以 2 mg(0.05 mL 或 40 mg/mL)注射溶液形式在玻璃体内(眼内)给药,根据标签中推荐的给药方案治疗上述病症的患者。
根据FDA的规定,可互换产品是一种生物制剂,其批准的依据是数据表明其与已批准的参考产品高度相似,并且两种产品之间没有临床意义上的差异。在任何给定的患者中,可互换产品有望产生与参考产品相同的临床结果。生物仿制药可以在药房替代参考产品,类似于仿制药替代品牌药物。
这两项批准都得到了临床对比试验的支持,以及使用物理化学测试和生物测定在分析水平上评估产品的研究。一项评估Yesafili(ClinicalTrials.gov标识符:NCT03610646)的3期研究比较了糖尿病和中心性糖尿病黄斑水肿患者的生物仿制药和Eylea。另一项纳入新生血管性AMD患者的3期研究(ClinicalTrials.gov标识符:NCT04450329)确立了Opuviz VS Eylea的疗效。
Yesafili和Opuviz的安全性与参考产品Eylea相似。治疗中最常见的不良反应包括结膜出血、眼睛疼痛、白内障、玻璃体脱离、玻璃体飞蚊症和眼压升高。
Yesafili 和 Opuiz 的安全信息
Yesafili 和 Opuviz 临床研究中观察到的副作用和不良事件与 Eylea 观察到的一致。这些副作用中最常见(≥5%)包括结膜出血、眼痛、白内障、玻璃体脱离、玻璃体飞蚊症和眼压升高。玻璃体液是一种透明的凝胶状物质,填充在眼睛的晶状体和视网膜之间的空间。
此外,禁忌症或警告和预防措施中包含的风险包括:
1.超敏反应
2.眼内炎(玻璃体和周围组织的炎症)、视网膜脱离以及伴有或不伴有闭塞的视网膜血管炎
3.眼压升高
4.血栓栓塞事件(血凝块)
参考来源:US Food and Drug Administration. FDA approves first interchangeable biosimilars to Eylea to treat macular degeneration and other eye conditions. May 20, 2024.
温馨提示:以上资讯来源于网络,由登越药业整理编辑(如有错漏,请帮忙指正),只为提供全球最新上市药品的资讯,帮助中国患者了解国际新药动态,仅供医护人员内部讨论,不作任何用药依据,具体用药指引,请咨询主治医师。
(责任编辑:登越药房)




