卡博特韦/利匹韦林,商品名为Cabenuva ,是一种用于治疗艾滋病毒/艾滋病的联合包装抗逆转录病毒药物。它包含卡博特韦和利匹韦林,每个包装有两个独立的注射瓶。
这种联合包装药物于 2021 年 1 月在美国获批用于医疗。这是 FDA 批准的首个针对 HIV 感染成人的注射完整治疗方案,每月注射一次。它也获准在加拿大使用。在欧盟,这两种药物是分开批准的,并且有不同的品牌名:Vocabria(用于卡博特韦)和Rekambys(用于利匹韦林)。
【生产企业】
ViiV Healthcare公司(由葛兰素史克(GSK)控股、辉瑞(Pfizer)和盐野义(Shionogi)持股的HIV/AIDS药物研发公司)
【规格】
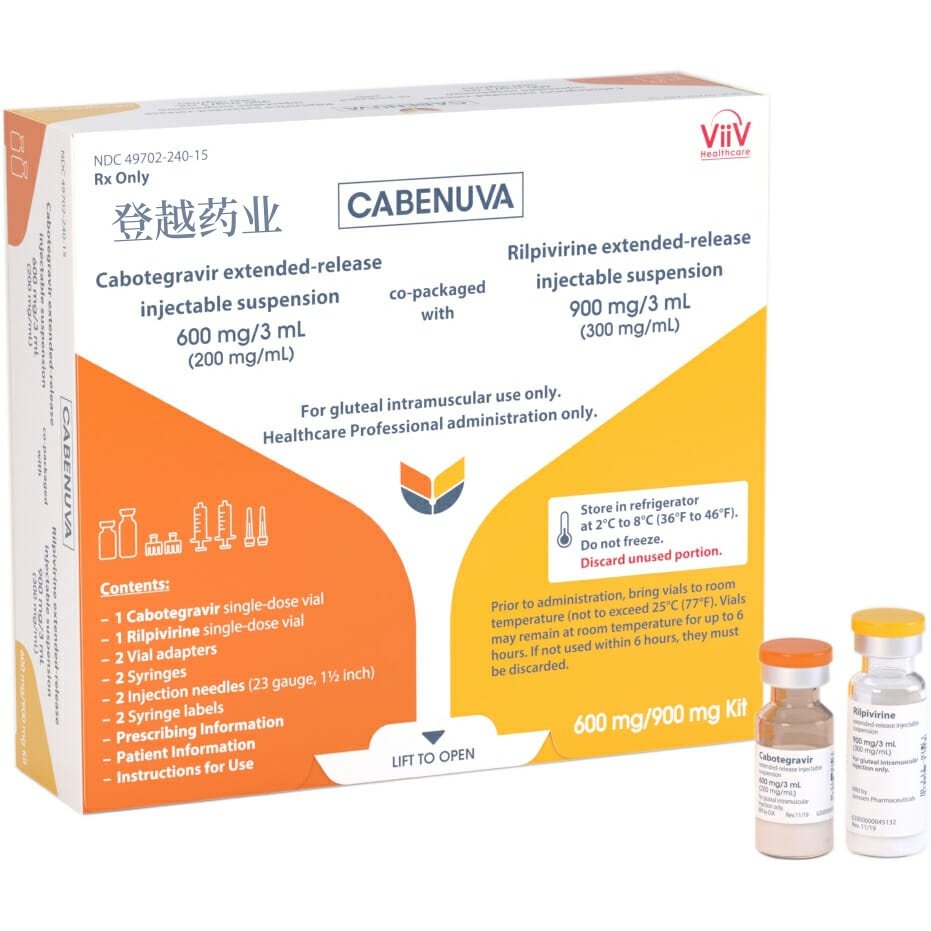
Cabenuva由一瓶Cabotegravir (白色至浅粉色缓释注射剂混悬液)和一瓶Rilpivirine(白色至灰白色缓释注射剂混悬液)组成,规格如下:
400-mg/600-mg装:由400 mg/2 mL (200 mg/mL)单剂量cabotegravir和600 mg/2 mL (300 mg/mL)单剂量rilpivirine组成。
600-mg/900-mg装:由600 mg/3 mL (200 mg/mL)单剂量cabotegravir和900 mg/3 mL (300 mg/mL)单剂量rilpivirine组成。
【商标】
Cabenuva
【通用名】
(Cabotegravir/Rilpivirine)卡博特韦/利匹韦林注射混悬液
【贮藏】:
1.将Cabenuva置于原包装纸箱中,储存在2-8℃的冰箱中,直到用前再取出。不要使药物冻结。请勿将药物与任何其他药物或稀释剂混合。
2.给药前,应将药瓶置于室温(不超过25℃)。在室温下,药瓶可以在纸箱中保留长达6小时;如果6小时内没有使用,必须丢弃。
3.一旦混悬药物被吸入相应的注射器,应尽快进行注射,但只能在注射器中保留长达2小时。如果超过2小时,必须丢弃药物、注射器和针头。
【Cabenuva 适应症】
作为 HIV-1 感染的完整治疗方案,用于替代目前的抗逆转录病毒治疗方案,适用于通过稳定的抗逆转录病毒治疗方案达到病毒学抑制(HIV-1 RNA <50 拷贝/毫升)且无治疗失败史、对卡博特韦或利匹韦林没有已知或疑似耐药性的患者。
【Cabenuva 剂量和用法】
成人
必须由医疗保健提供者管理。在同一次就诊时,在不同的臀肌注射部位(在相对侧或相距 2 厘米)进行每次肌肉注射;最好是臀大肌部位。请勿通过任何其他途径或解剖部位给药。≥12 岁(≥35 公斤):在开始使用之前,可以考虑给予口服引导剂量(使用 Vocabria 和 Edurant)约 1 个月(≥28 天)以评估耐受性,或者可以直接进行 Cabenuva 注射,而不使用口服引导剂量。选择合适的注射剂量选项。每月给药:开始单次注射 600mg/900mg(在当前抗逆转录病毒疗法或口服引导的最后一天,如果使用),然后继续每月单次注射 400mg/600mg 一次。或者,每 2 个月给药一次:开始单次注射 600mg/900mg(在当前抗逆转录病毒疗法的最后一天或口服引导剂,如果使用)连续 1 个月间隔 2 个月(第 1 个月和第 2 个月),然后每 2 个月继续注射一次(从第 4 个月开始)。两种方案:可在预定日期前或后最多 7 天进行注射,以接受每月或每 2 个月注射。从每月注射改为每 2 个月注射,每 2 个月注射改为每月注射,错过注射:请参阅完整标签。
孩子们
<12 岁或 <35 公斤:未确定。
【Cabenuva 警告/注意事项】
如果出现超敏反应,请立即停药。监测注射后反应;如果发生,请适当治疗。潜在的肝脏疾病或转氨酶显著升高。监测肝功能;如果怀疑有肝毒性,请停药。如果出现抑郁症状,请立即评估。长效特性:残留药物浓度可能保持≥12个月。如果怀疑有病毒学失败,请改用替代疗法。严重肝功能不全。严重肾功能不全或 ESRD:监测。老年人。怀孕:可能接触胎儿。哺乳期母亲:参见完整标签。
【Cabenuva 药代动力学】
吸收
达到最大血浆浓度的时间(中位数):7 天(卡博特韦);3-4 天(利匹韦林)。
分配
血浆蛋白结合率:>99.8%(卡博替韦);99.7%(利匹韦林)。血液与血浆的比率:0.52(卡博替韦);0.7(利匹韦林)。脑脊液与血浆的浓度比率(中位数):0.003(卡博替韦);0.01(利匹韦林)。
代谢
卡博特韦:UGT1A1、UGT1A9(次要);利匹韦林:CYP3A。
消除
卡博特韦:粪便(59%)、肾脏(27%);利匹韦林:粪便(85%)、肾脏(6%)。半衰期:5.6-11.5 周(卡博特韦);13-28 周(利匹韦林)。
【Cabenuva 不良反应】
注射部位反应、发热、疲劳、头痛、肌肉骨骼疼痛、恶心、睡眠障碍、头晕、皮疹;肝毒性、抑郁症。
温馨提示:以上资讯由登越药业整理编辑(如有错漏,请帮忙指正),只为提供全球最新上市药品的资讯,帮助中国患者了解国际新药动态,仅供医护人员内部讨论,不作任何用药依据,具体用药指引,请咨询主治医师。
(责任编辑:登越药房)




